تفاوت های نظریه برخورد و حالت گذار در شیمی
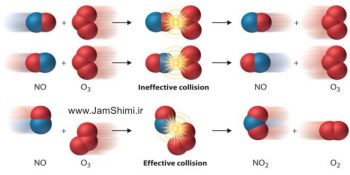
بر اساس نظریه برخورد هنگامی بین دو ذره یک واکنش شیمیایی رخ می دهد که علاوه بر انرژی کافی برخورد ذره ها با یکدیگر، از جهت برخورد مناسب و تعداد برخورد مناسب نیز برخوردار باشد. نظریه های سینتیک شیمیایی به طور کلی به دو دسته طبقه بندی می شوند که نظریه حالت گذار و نظریه برخورد نام دارد. گرچه اساس هر دو نظریه، برخورد بین ذرات واکنش دهنده است ولی میان آن ها تفاوت های بنیادی وجود دارد که در ادامه از جم شیمی به بررسی تفاوت های نظریه برخورد و حالت گذار در شیمی می پردازیم.
تفاوت های نظریه برخورد و حالت گذار
- نظریه برخورد برای واکنش ها در فاز گازی کاربرد دارد در حالی که نظریه حالت گذار علاوه بر فاز گازی در فاز محلول نیز قابل استفاده است.
- در نظریه برخورد ذره های واکنش دهنده به صورت گوی های سخت در نظر گرفته می شوند اما در نظریه حالت گذار ذره های واکنش دهنده ضمن مبادله انرژی بر یکدیگر اثر می گذارند.
- در نظریه برخورد فقط حرکت های انتقالی ذرات در نظر می گیریم در حالی که در نظریه حالت گذار حرکت های چرخشی و ارتعاشی ذره های واکنش دهنده نیز در نحوه انجام واکنش تاثیر دارند.
- در نظریه برخورد پس از برخورد موثر واکنش انجام می گیرد اما در نظریه حالت گذار واکنش دهنده ها پس از برخورد در کنار هم قرار می گیرند و پیچیده فعال یا همان کمپلکس تشکیل می دهند.
- در نظریه برخورد می توان گفت انرژی فعال سازی وجود دارد ولی نمی توان مقدار آن را محاسبه کرد ولی در نظریه حالت گذار مقدار انرژی فعال سازی را می توان محاسبه کرد.
- در نظریه برخورد حالت گذار وجود ندارد.
در نظریه برخورد ذره های واکنش دهنده به صورت گوی های سخت در نظر گرفته می شوند و یک واکنش شیمیایی زمانی صورت می گیرد که بین ذره های واکنش دهنده برخورد مناسب و موثری صورت پذیرد. یک برخورد موثر سه ویژگی دارد:
1- تعداد برخوردها
2- جهت گیری مناسب ذره ها هنگام برخورد
3- انرژی مناسب ذره ها هنگام برخورد
نتیجه گیری: از میان همه برخوردها فقط تعداد معدودی منجر به انجام واکنش می شوند. این تعداد باید دو ویژگی داشته باشند: 1- جهت گیری مناسب 2- انرژی کافی
ایرادهای نظریه برخورد:
نظریه برخورد ذرات را جدا و مستقل از هم فرض می کند و این فرض در واقع فقط در فاز گازی صادق است. لذا نظریه برخورد در سایر فازها ( محلول، جامد یا مایع) قابل استفاده نیست. همان طور که گفته شد در نظریه برخورد، ذرات واکنش دهنده به صورت گوی های سخت در نظر گرفته می شوند که برخوردی کشسان دارند، منظور از برخورد کشسان برخوردی است که در آن هیچ انرژی صرف تغییر شکل ساختار گوی ها نمی شود.
امروزه می دانیم که برخورد بین اتم ها کشسان نیست زیرا اتم ها بر یکدیگر اثر می گذارند مانند هم پوشانی در پیوند کووالانسی. در این نظریه تنها حرکت انتقالی ذرات در نظر گرفته شده و به تاثیر حرکات چرخشی و ارتعاشی در واکنش توجهی نشده است. هم چنین با استفاده از نظریه برخورد می توان گفت انرژی فعال سازی وجود دارد اما مقدارش را نمی توان محاسبه کرد.







