الكتروليز
الكتروليز
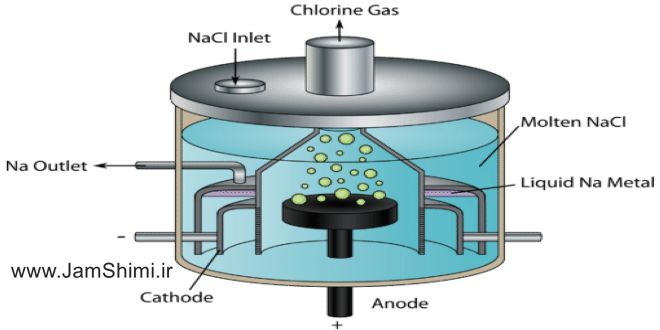
فرايندی که طی آن انرژی الکتريکی تبديل به انرژی شيميايی می شود،را الکتروليز می گويند .اين پديده درسلولی به نام سلولهای الکتروليتی انجام می گيرد.وشامل دوالکترود است که هريک توسط يک رشته سيم رسانا به يک قطب باتری متصل شده اند ودرمحلول الکتروليت مناسب قرار می گيرند .واکنشی که درسلول الکتروليتی انجام می گيرد انرژی خواه بوده ودرنتيجه محتوای انرژی فراورده بالاترازواکنش دهنده ها می باشد .باتری قرارگرفته درمدار نقش يک پمپ الکترون راداردکه با صرف کارالکتريکی ،الکترون را از آند گرفته ودراختيار کاتد قرار می دهد.
بايد درنظر داشته باشيد که :
۱ـ در کاتد همواره عمل کاهش صورت می گيرد با اين تفاوت که درسلولهای گالوانی نقش قطب مثبت داشته، اما در سلولهای الکتروليتی به قطب منفی مولد متصل می شود .
۲ـ درآند که همواره عمل اکسايش انجام می گيرد درسلول گالوانی نقش قطب منفی را دارد در حالی که در سلول الکتروليتی بايد به قطب مثبت متصل شود.
ازالکتروليزبرای آبکاری بافلز،تصفيه فلزها،استخراج فلز،تجزيه مواد ….استفاده می شود.
باکليک دراینجا توانايی انجام چند آزمايش جالب را کسب می نماييد