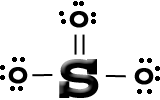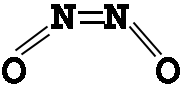دانلود نمونه سوال شیمی2 بخش چهارم

برای دانلود نمونه سوال شیمی2 بخش چهارم از سایت جم شیمی به ادامه مطلب مراجعه کنید
۳- ساختار لوویس گونه های زیر را رسم کنید .
|
C3H8
|
So3
|
|
No+
|
۴- کدام ساختار زیر برای NH3O درست می باشد؟
|
|
|
۵- عدد اکسایش اتم نیتروژن را در ترکیبهای زیر مشخص کنید.
HNO3 : +1 + N + (-2*3) = 0 –> N= +5
NOCl : N – 2 -1 = 0 –> N = +3
NH4Cl : N + (4*1) – 1 = 0 –> N = -3
NaN3 : 1 + (3*N) = 0 –> N = – 1/3
Al(NO2)3 : 3 + (3*N ) + (-2*2*3) = 0 –> N = +3
6- پیوندهای مقابل را براساس افزایش قطبیت مرتب کنید.
H_H و H_Cl و H_O و F_H
اختلاف الکترونگاتیوی هر دو اتم تشکیل دهنده ی پیوند را محاسبه می کنیم
|
از بالا به پایین قطبیت افزایش میابد |
Cl_H ۳/۰-۲/۱ = ۰/۹ O_H ۳/۵ – ۲/۱ =۱/۴ F_H ۴ – ۲/۱ = ۱/۹ |
|
پیوند کووالانسی |
H_H ۲/۱-۲/۱ = ۰ |
۷- چرا در ترکیب OF2 ، اتم اکسیژن را در سمت چپ ولی در ترکیب Br2O آن را در سمت راست فرمول ترکیب می نویسیم؟
زیرا الکترو نگاتیوی O از F کمتر است و از Br بیشتر است.
۸- چرا تشکیل پیوند گرماده و شکستن آن گرماگیر است .
زیرا اتمها وقتی با هم پیوند تشکیل می دهند، حالت پایداری پیدا کرده و به سطح انرژی پائین تری می رسند. ( در این حالت انرژی آزاد می شود) . ولی هنگامی که می خواهیم اتمهای یک پیوند را از هم جدا کنیم باید انرژی مصرف کنیم تا پیوند را بشکنیم ( مقدار این انرژی برابر با همان انرژی است که در هنگام تشکیل پیوند آزاد شده بود)
۹- ساختار لوویس CH3OH (متانول) و C2H5OH (اتانول ) را رسم کنید.
|
اتانول |
متانول |
۱۰- آرایش لوویس مولکول های زیر را رسم کنید
|
COCl2
|
N2O2
|
|
O2F2
|
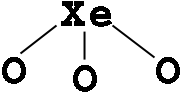
XeO
|