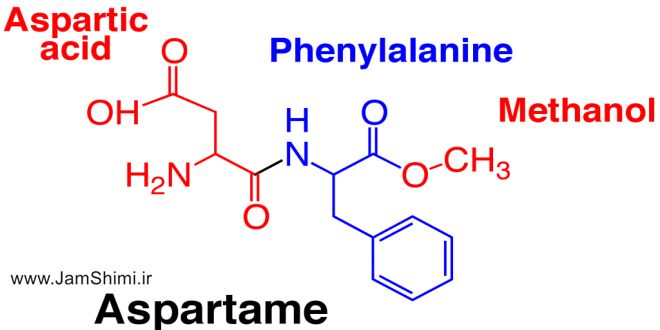
شعاع اتمی وروند تغییرات آن در جدول تناوبی عناصر

شعاع کووالانسی
به نصف فاصله بین هسته ای دو اتم مشابه در یک مولکول دو اتمی هم نام/شعاع کووالانسی می گویند.نصف فاصله هسته ها در یک مولکول دو اتمی جور هسته را شعاع کووالانسی می گویندبا تقسیم کردن طول پیوند برعدد ۲،شعاع اتمی که شعاع کووالانسی هم نامیده میشود بدست میآیدواحد شعاع کووالانسی pm پیکومتر است
روند تغییرشعاع اتمی در یک گروه:
شعاع اتمی عنصر ها در هر گروه از جدول تناوبی از بالا به پایین افزایش میابد:
زیرا :
*ازبالا به پایین در یک گروه جدول /به ازای هر تناوب یک لایه الکترونی جدید به تعدادلایه های الکترونی عنصر ها افزوده میشود.با زیاد شدن تعداد لایه هایالکترونی/شعاع اتمی نیز افزایش میابد.به عبارت دیگر الکترون ها در فاصله دورتری نسبت به هستهقرار می گیرند.
*دلیل دیگر برای افزایش شعاع اتمی این است که با افزایش عدد اتمی در یک گروه/تعداداربیتال های پرشده بین هسته و لایه های الکترونی بیرونی اتم افزایش میابد.وجودالکترون ها در اربیتال های درونی و اثرپوششی آنها بر الکترون های بیرونی/باعث افزایشفاصله الکترون های بیرونی از هسته یا به عبارتی افزایش شعاع اتمی میشود.
روند تغییرشعاع اتمی در یک دوره:
بطور کلی شعاع کووالانسی در جدول تنابی از چپ به راست کاهش می یابد.در یک تناوب ازچپ به راست تعداد لایه های الکترونی ثابت است ولی بار مثبت هسته افزایش می یابد درنتیجه الکترون های بیرونی را بیشتر به سوی خود کشیده و اتم کوچکتر می شود